PRIMERA LEY DE LA TERMODINÁMICA
La primera ley de termodinámica También conocida como principio de conservación de la energía, establece que la energía ni se crea ni se destruye, solo se transforma. Ejemplo, permite definir el calor como la energía necesaria que debe intercambiar el sistema para compensar las diferencias entre trabajo y energía interna. La termodinámica fue propuesta por NICOLAS LEONAR SADI CARNOT en 1824, en la que expuso los dos primeros principios de la termodinámica. Esta obra fue postergada por los científicos de su época, y más tarde fue utilizada por Rudolf Clausius y Lord Kelvin para formular, de una manera matemática, las bases de la termodinámica.
La primera ley de termodinámica También conocida como principio de conservación de la energía, establece que la energía ni se crea ni se destruye, solo se transforma. Ejemplo, permite definir el calor como la energía necesaria que debe intercambiar el sistema para compensar las diferencias entre trabajo y energía interna. La termodinámica fue propuesta por NICOLAS LEONAR SADI CARNOT en 1824, en la que expuso los dos primeros principios de la termodinámica. Esta obra fue postergada por los científicos de su época, y más tarde fue utilizada por Rudolf Clausius y Lord Kelvin para formular, de una manera matemática, las bases de la termodinámica.
Que aplicada a la termodinámica teniendo en cuenta el criterio de signos termodinámico, queda de la forma:



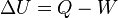

No hay comentarios:
Publicar un comentario